Biologická léčiva jsou makromolekulární látky, peptidy, bílkoviny nebo segmenty nukleových kyselin, při jejichž přípravě se používají živé organismy nebo jejich produkty.
Výroba bioléčiv patří mezi nejpřísněji regulované procesy, které zajištují vznik vysoce účinného a funkčního produktu.
Pomocí analýzy rizik se provádí identifikace kritických proměnných (CQA - Critical Quality Attributes), ovlivňujících finální kvalitu výrobku. CQA jsou fyzikální, chemické, biologické a mikrobiologické vlastnosti a charakteristiky přípravku, které mají splňovat určený limit, rozmezí a distribuci tak, aby byla zajištěna požadovaná kvalita.
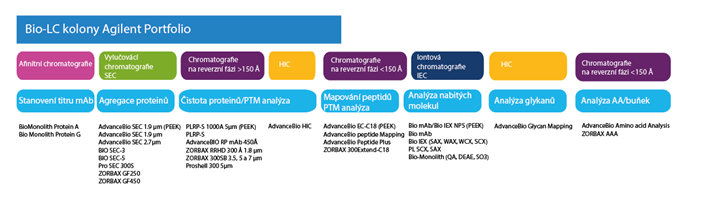
Agilent nabízí celou řadu chromatografických LC kolon pro monitoring a identifikaci kritických proměnných ve farmaceutickém průmyslu biologických léčiv.
Kolony Agilent Bio-Monolith Protein A a Protein G pro stanovení titru protilátek
Afinitní chromatografie je metoda izolace biologicky aktivních látek, která využívá vysoce specifických molekulárních interakcí mezi proteiny (např. antigen/protilátka). Stacionární fáze kolon se připravují navázáním afinitního ligandu na pevný nosič. Agilent nabízí několik výjimečných afinitních produktů, včetně monolitických kolon pro izolaci a kvantifikaci monoklonálních protilátek (mAb).
Kolony Agilent Bio-Monolith Protein A a Protein G jsou navrženy pro analytickou separaci všech lidských a myších podtříd Imunoglobulinu G (IgG). Poskytují rychlé a přesné kvantifikace titru protilátky a přečištění jejího malého množství pro další charakterizaci např. pomocí hmotnostní spektrometrie. Tyto monolitické kolony jsou tvořeny z poly(glycidyl methakrylát-ko-etylen dimetkrylátu) - s vrstvou Proteinu A nebo Proteinu G, izolovaného ze Staphylococcus aureus.

Kolony jsou kompatibilní s HPLC a UHPLC systémy, včetně Agilent 1100, 1200 a 1260 Bio-inertní kvartérní LC.
Dostupné online na e-shopu zde
Aplikační listy:
- Bio-Monolith Protein G column - More Options for mAb Titer Determination
- Robust, Reliable Recombinant Protein A Monolith Column for Antibody Titer Determination
- mAb Titer Analysis with the Agilent Bio-Monolith Protein A Column
- Cell Culture Optimization Using an Agilent Bio-Monolith Protein A Column and LC/MS
- Cell Clone Selection Using the Agilent Bio-Monolith Protein A Column and LC/MS
- Reducing Cycle Time for Quantification of Human IgG Using the Agilent Bio-Monolith Protein A HPLC Column
- Agilent Bio-Monolith Protein A Monitors Monoclonal Antibody Titer from Cell Cultures
- Agilent AdvanceBio Desalting-RP Cartridges for Online Desalting in 2D-LC/MS mAb Analysis
- Protein A Affinity IgG Capture Followed by AdvanceBio SEC Aggregation Analysis
- Biomolecule characterization workflow agilent bio-monolith protein a and protein g affinity columns
Kolony AdvanceBio SEC - pro monitorování agregace proteinů
Profil nečistot bioterapeutik má v bezpečnosti léčiv stále větší význam. Přestože jsou agregáty přítomny v extrémně nízkých koncentracích, mohou mít velký dopad na kvalitu produktu. Pro kvantifikaci a monitorování agregace proteinů, oligonukleotidů a dalších komplexních biopolymerů, např. pro analýzu analogů inzulinu, je proto chromatografie založená na dělení dle velikosti částic (SEC - Size Exclusion Chromatography) ideální metodou.
Výběrem sorbentu o určité velikosti pórů ovlivňujeme rozsah molekulových hmotností analytů, které můžeme měřit na zvoleném sorbetu (tzv. vylučovací limit kolony).
Kolony AdvanceBio SEC 1.9 μm a 2.7 µm pro stanovení agregace mAb a fragmentovou analýzu. Tyto kolony zmírňují interakce analytů s povrchem z nerezové oceli. Vyznačují se nízkým vnitřním průměrem 2.1 mm pro průtoky 0.05 až 0.10 ml/min a jsou ideální pro náročné analýzy proteinů. Jejich inertní hydrofilní povrch umožňuje používat nižší koncentraci těkavých aditiv
v mobilní fázi, což vede k minimalizaci nespecifických interakcí. Kolony z nerezové oceli PEEK-lined neobsahují aktivní kovová místa, což snižuje potřebu prekondicionovaní kolony - a šetří čas a množství vzorků.

Agilent Bio SEC-3 - kolony se sférickými 3µm částicemi, pokrytými hydrofilní vrstvou (100 Å, 150 Å a 300 Å).
Agilent Bio SEC-5 - kolony se sférickými 5µm částicemi, pokrytými hydrofilní vrstvou (100 Å, 150 Å, 300 Å, 500 Å, 1000 Å a 2000 Å).
Dostupné online na eshopu zde
Aplikační listy:
- Agilent Biocolumns - Critical Quality Attributes - Aggregate Compendium
- Agilent AdvanceBio SEC columns for peptides and proteins
- Analysis of Antibody Fragment-Drug Conjugates Using an Agilent AdvanceBio SEC 120 Å 1.9 µm PEEK-Lined Column
- Surmounting the Challenges of Bispecific Antibody Characterization
- Analysis of Nanobodies Agilent AdvanceBio SEC 120 Å 1.9 μm and AdvanceBio HIC Columns
- High Resolution Size Exclusion Chromatography Analysis of Small Therapeutic Proteins
- High-Resolution, High-Throughput Size Exclusion Chromatography Analysis of Monoclonal Antibodies Using an Agilent AdvanceBio SEC 200 Å 1.9 µm Column
- Sensitive Native Mass Spectrometry of Macromolecules Using Standard Flow LC/MS
- High Performance Size Exclusion Chromatography for Analysis of Covalent High Molecular Weight Insulin
- Size Exclusion Chromatography Analysis of a Monoclonal Antibody and Antibody Drug Conjugate Using an Agilent AdvanceBio SEC 200 Å 1.9 µm Column
- Size Exclusion Chromatography of Biosimilar and Innovator Insulin
- Characterization of mAb aggregation
- Size Exclusion Chromatography in the Presence of an Anionic Surfactant
- Fast, High-Resolution Size Exclusion Chromatography of Aggregates in Biotherapeutics
- Separate and Quantify Rituximab Aggregates and Fragments with High-Resolution SEC
- Size Exclusion Chromatography Analysis of Antibody Drug Conjugates
- Protein A Affinity IgG Capture Followed by AdvanceBio SEC Aggregation Analysis
- Online 2D-LC Characterization of Monoclonal Antibodies with Size Exclusion and Weak Cation Exchange Chromatography
- Analysis of PEGylated Proteins with Agilent AdvanceBio SEC columns
- Quantitation of mAb and ADC Aggregation Using SEC and an Aqueous Mobile Phase
- Comparison of Biosimilar and Innovator Monoclonal Antibody Rituximab Using the Agilent 1260 Infinity Bio-inert LC System and Agilent OpenLAB Match Compare Software
- Does Tween 20 affect Monoclonal Antibody Separation?
- Choosing the Right Calibration for the Agilent Bio SEC-3 Column
- Analysis of Antibody Drug Conjugates Using SEC and Mass Spectrometry
- Defining the Optimum Parameters for Efficient Size Separations of Proteins
- Characterization of monoclonal antibodies on the Agilent 1260 Infinity Bio-inert Quaternary LC by Size Exclusion Chromatography using the Agilent BioSEC columns
- Fast Separation of Monoclonal Antibody and Dimer by SEC with Agilent Bio SEC
- Multiple Detector Approaches to Protein Aggregation by SEC
Kolony s reverzní stacionární fází (SF), s částicemi >150 Å pro stanovení intaktních proteinů
Kolony Agilent PLRP-S 1000 Å 5 μm
- fáze na bázi poly(styrene/divinylbenzene) pro separaci biomolekul
- teplotně i chemicky velice stabilní, rozsah pH 1 – 14, teplota až 200 °C
- zrnitost od 3 do 50 µm

Absence zbytkových silanolových skupin umožňuje zlepšení tvaru píku. Hardware lemovaný PEEK kolony navíc minimalizuje riziko artefaktů - jako je oxidace - v důsledku sekundárních kovových interakcí.
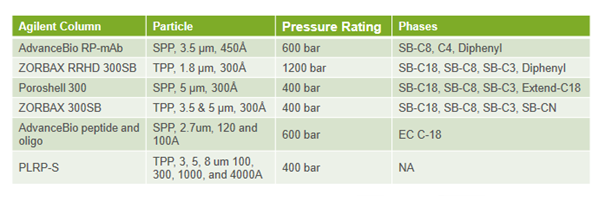
AdvanceBio RP-mAb – pro analýzu monoklonálních protilátek
ZORBAX RRHD – 300A – pro UHPLC analýzy
- max. tlak 1200bar – optimalizované pro UHPLC 1290 Infinity, vhodné pro další UHPLC/UPLC přístroje
- 12 selektivních fází, zrnitost 1.8 µm
- snadný přechod z 3.5 a 5 µm díky stejné selektivitě fází

ZORBAX 300StableBond
Kolony Agilent ZORBAX 300Å StableBond jsou ideální volbou pro reprodukovatelné separace proteinů a peptidů. Tyto kolony jsou k dispozici ve čtyřech stacionárních fázích: C18, C8, C3 a Diphenyl.
- velikost pórů 300 Å poskytuje vysokou účinnost separace
- čtyři různé stacionární fáze - 300SB-C18, 300SB-C8, 300SB-C3 a 300Extend-C18
- kolonu Poroshell 300Extend-C18 lze použít při pH od 2 do 11
- možná separace peptidů a proteinů až do 500 - 1 000 kDa při tlaku 400/600 bar

Aplikační listy:
- Ion-Pair Reversed-Phase Purification of De-Protected Oligonucleotides – Choice of Pore Size
- Use Temperature to Enhance Oligonucleotide Mass Transfer and Improve Resolution in Ion-Pair RP HPLC
- Improved Column Lifetime with Thermally Stable Polymer Columns for Oligonucleotide Ion-Pair RP HPLC
- Efficient Monoclonal Antibody and Antibody Drug Conjugate Desalting Prior to Mass Spectrometry using AdvanceBio Desalting-RP Cartridges
- Cell Clone Selection Using the Agilent Bio-Monolith Protein A Column and LC/MS
- 2D-LC as automated desalting tool for MSD analysis
- Agilent AdvanceBio Desalting-RP Cartridges for Online Desalting in 2D-LC/MS mAb Analysis
- Application of AdvanceBio Desalting - RP Cartridges for LC/MS Analysis of mAbs
- Characterize Fab and Fc Fragments by Cation-exchange Chromatography
- LC/MS Analysis of Intact Therapeutic Monoclonal Antibodies Using AdvanceBio RP-mAb
- Fast and High Resolution Analysis of Intact and Reduced Therapeutic Monoclonal Antibodies
- Identifying Monoclonal Antibody Mutation Sites Using 2D-LC with Q-TOF LC/MS
- Separation of Native Monoclonal Antibodies and Identification of Charge Variants
- Characterization of Glycosylation in the Fc Region of Therapeutic Recombinant Monoclonal Antibody
- Intact Protein Analysis Using an Agilent 6550 Q-TOF Mass Spectrometer
- Analysis of Monoclonal Antibody (mAb) Using Agilent 1290 Infinity LC System Coupled to Agilent 6530 Accurate-Mass Quadrupole Time-of-Flight (Q-TOF)
- Accurate Mass Measurement for Intact Proteins using ESI-oa-TOF
- Protein Confirmation Using the LC/MSD TOF and the Agilent TOF Protein Confirmation Software
- Fast Separation of Large and Heterogeneous Proteins Using ZORBAX Poroshell C18, C8, and C3 Phases.
- Effect of Flow Rate on Ultra-fast Separations of Proteins on Porous and Superficially Porous Particle Columns
- Using Poroshell 300SB-C18 for High-Sensitivity, High-Throughput Protein Analysis on the Agilent LC/MSD
- Fast Protein Separations Using Agilent Poroshell 300
- LC/MS of Intact Adeno-Associated Virus (AAV) Capsid Proteins for Product Identity
- Characterization of Viral Vector Particles Using the Agilent 6545XT AdvanceBio LC/Q-TOF
Kolony s reverzní stacionární fází (SF), s částicemi <150 Å pro mapování peptidů
Mapování peptidů lze použít ke komplexní identifikaci primární struktury proteinu, která umožnuje identifikaci fragmentů generovaných při štěpení proteinů pomocí enzymů, např. trypsinu. Různé proteiny poskytují různé peptidové „otisky prstů“.
AdvanceBio Peptide Mapping - Peptidové mapování
Kolony HPLC jsou uřčený pro identifikaci proteinů a stanovení posttranslačních modifikací. Kolony umožňují rychlou identifikaci aminokyselinové substituce/modifikace v primární sekvenci proteinu. Kolony jsou povrchově porézní a mají velikost pórů 120 Å, což je optimální pro analýzu peptidů produkovaných enzymatickým štěpením proteinů.
AdvanceBio 2.7 μm EC-C18
AdvanceBio Peptide Plus
ZORBAX 300Extend-C18
AdvanceBio Amino Acid Analysis (AAA)
Aplikační listy:
- High-Resolution Mapping of Drug Conjugated Peptides in an ADC Digest
- Comparison of Biosimilar and Innovator Monoclonal Antibody Rituximab Using the Agilent 1260 Infinity Bio-inert LC System and Agilent OpenLAB Match Compare Software
- High Resolution Glycopeptide Mapping of EPO Using an Agilent AdvanceBio Peptide Mapping Column
- Separation of IgG Glycopeptides using HILIC-LC/MS in Comparison to RP-LC/MS
- Peptide Mapping of Innovator and Biosimilar Monoclonal Antibody
- Peptide Mapping: A Quality by Design (QbD) Approach
- Making Peptide Mapping Routine with the Agilent 6545XT AdvanceBio LC/Q-TOF
- Reversed-phase LC primary structure characterization workflow
- High Resolution and Rapid Peptide Mapping of Monoclonal Antibody Using an Agilent 1290 Infinity UHPLC and an Agilent 6550 iFunnel Q-TOF LC/MS System
- Fast and Efficient Peptide Mapping of a Monoclonal Antibody (mAb): UHPLC Performance with Superficially Porous Particles
- Analysis of Amino Acids Derived Online Using an Agilent AdvanceBio AAA Column
- Determination of Amino Acid Composition of Cell Culture Media and Protein Hydrosylate Standard
Pro bližší informace o HPLC BIO kolonách nás neváhejte kontaktovat na e-mail info@hpst.cz
Článek byl publikován na LabRulezLCMS 25. 8. 2021





